Det har længe været kendt, at alle molekyler har to lige og modsatte ladninger, som er adskilt med en bestemt afstand. I tilfælde af sådanne polære molekyler falder centrum af negativ ladning ikke sammen med centrum af positiv ladning. Omfanget af polaritet i sådanne kovalente molekyler kan beskrives ved udtrykket Dipole Moment, som i det væsentlige er målet for polaritet i en polær kovalent binding.
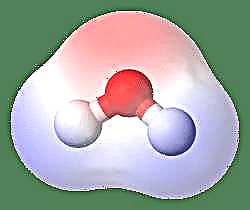
Det enkleste eksempel på en dipol er et vandmolekyle. Et molekyle af vand er polært på grund af den ulige deling af dets elektroner i en "bøjet" struktur. Vandmolekylet danner en vinkel med brintatomer i spidserne og ilt i toppunktet. Da ilt har en højere elektronegativitet end brint, har siden af molekylet med oxygenatomet en delvis negativ ladning, mens brintet i midten har en delvis positiv ladning. På grund af dette peger retning af dipolmomentet mod iltet.
På fysikens sprog er det elektriske dipolmoment et mål for adskillelse af positive og negative elektriske ladninger i et ladningssystem, det vil sige et mål for ladningssystemets samlede polaritet - dvs. adskillelsen af molekylernes elektriske ladning, som fører til en dipol. Matematisk, og i det enkle tilfælde af to punktladninger, en med ladning + q og en med ladning? Q, kan det elektriske dipolmoment p udtrykkes som: p = qd, hvor d er forskydningsvektoren, der peger fra negativ ladning til den positive ladning. Således peger den elektriske dipolmomentvektor p fra den negative ladning til den positive ladning.
En anden måde at se på det er at repræsentere Dipole Moment ved det græske bogstav m, m = ed, hvor e er den elektriske ladning og d er adskillelsesafstanden. Det udtrykkes i enhederne til Debye og skrives som D (hvor 1 Debye = 1 x 10-18e.s.u cm). Et dipolmoment er en vektormængde og er derfor repræsenteret af en lille pil med en hale i det positive center og hoved, der peger mod et negativt centrum. For et vandmolekyle er Dipol-momentet 1,85 D, hvorimod et molekyle saltsyre er 1,03 D og kan repræsenteres som:
Vi har skrevet mange artikler om dipol-øjeblik for Space Magazine. Her er en artikel om, hvad vand er lavet af, og her er en artikel om molekyler.
Hvis du gerne vil have mere information om dipol-øjeblik, kan du tjekke disse artikler fra Hyperphysics og Science Daily.
Vi har også optaget en hel episode af Astronomy Cast alt om molekyler i rummet. Lyt her, afsnit 116: Molekyler i rummet.
Kilder:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule